היפראנדרגוניזם
היפראנדרוגניזם הוא מחלה אנדוקרינית המאופיינת ברמות גבוהות של אנדרוגנים, וגורמת להפרעה במיוחד אצל נשים. התסמינים עלולים לכלול אקנה, נשירת שיער בקרקפת, שיער מוגבר בגוף או בפנים, וסת נדירה או נעדרת. הסיבה בכ-70% מהמקרים היא תסמונת השחלות הפוליציסטיות. גורמים אחרים כוללים היפרפלזיה של יותרת הכליה, תסמונת קושינג, סוגים מסוימים של סרטן ותרופות מסוימות.
| תחום |
מיילדות וגינקולוגיה |
|---|---|
| תסמינים |
הירסוטיזם, אקנה, אל-וסת |
| קישורים ומאגרי מידע | |
| MeSH | D017588 |
| סיווגים | |
| ICD-10 |
E28.1 |
| ICD-11 |
5A80.0 |
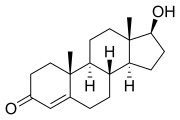 | |
| טסטוסטרון אנדרוגן חשוב בהתפתחות היפר אנדרגוניזם, רמות גבוהות בגוף מהוות גורם מסכן למחלה. | |
| שם סיסטמטי | (8R,9S,10R,13S,14S,17S)- 17-hydroxy-10,13-dimethyl- 1,2,6,7,8,9,11,12,14,15,16,17- dodecahydrocyclopenta[a] phenanthren-3-one |
|---|---|
סימנים ותסמינים
עריכהכ-5 עד 10% מהנשים בגיל הפוריות סובלות מהיפר-אנדרוגניזם. היפראנדרוגניזם בא לידי ביטויי גם בגברים, אך בולט יותר בנשים מכיוון שרמות גבוהות של אנדרוגנים מדגישות את הויריליזציה (אוסף תכונות המאפיינות גברים כגון: כמבנה גוף, קול עמוק, שעירות, וכו'). מכיוון שהיפראנדרוגניזם מאופיין בעלייה ברמות הורמוני המין הגבריים, תסמינים של היפר-אנדרוגניזם אצל גברים לרוב זניחים שכן נחשבים למראה הטבעי. בדרך כלל היפר-אדרוגניות מאובחנת בקרב נשים בגיל הנעורים[1](גיל ההתבגרות מתקדם) . הסקירה הרפואית מורכבת מבדיקת אגן, הבחנת בתסמינים חיצוניים ובדיקת דם להערכת רמות אנדרוגן.
- הירוטיסם -צמיחת שיער טרמינלי, שיער הגוף.
- אלופציה - התקרחות
- מראה גברי
- הידרדניטיס סופורטיבה
- תסמונת השחלות הפוליציסטיות
- אוליגומנוריאה – אי סדירות בווסת
- אקנה
- השמנת יתר
- עקרות
- שינויי במיתרי הקול
- עור שמנוני
- סבוריאה דרמטיטיס
- ליבידו - חשק מיני
- סוכרת מסוג 2
נשים
עריכההיפראנדרוגניזם, כאשר רמות הטסטוסטרון הן גבוהות במיוחד, עלול לגרום לתופעות חמורות בנשים אם לא מותאם טיפול. רמת טסטוסטרון גבוה נמצאה כאחת הסיבות להשמנה, יתר לחץ דם, אמנוריאה (הפסקת הווסת) ופוגעת בהליך הביוץ, מה שעשוי להוביל לעקרות. הסימנים הבולטים יותר של היפר-אנדרגוניזם זו צמיחת שיער טרמינלי (באזור הבטן, חזה וכו), התקרחות, אקנה, שינויי הקול. היפר-אנדרוגניזם גורם להתפתחות הטולרנטיות לאינסולין, מה שעלול להוביל לסוכרת מסוג 2, ולדיסליפידמיה, כמו כולסטרול גבוה. כמו כן, נראה כי ישנה השפעה פסיכולוגית ניכרת על האינדיבידואל בעקבות הסימפטומים. דבר שלעיתים מוביל לחרדה חברתית, דיכאון וביטחון עצמי ירוד ,[2] במיוחד בקרב נערות מתבגרות ונשים צעירות.[3]
גברים
עריכהאף על פי כי היפראנדרוגניזם אינו שכיח בקרב גברים, נערכו מחקרים שבדקו את השפעות של רמות טסטוסטרון גבוהות גם בגברים. מחקר הראה כי אף על פי שברוב הגברים לא חלו שינויים עקב העלייה ברמות הטסטוסטרון, היו מקרים בהם המשתתפים סבלו ממקרי תוקפנות לא אופיינית להם. רמות גבוהות של טסטוסטרון אצל גברים לא נמצאו בעלות השפעה ישירה על אישיותם, אך נצפו מקרים של תוקפנות פתאומית.[4] תסמינים נוספים כוללים: חשק מיני מוגבר, מסת שרירים גדולה, צפיפות עצם גבוהה, רמת כולסטרול גבוה, ספירת זרע נמוכה, לחץ דם גבוה וכתוצאה מכך סיכוי גדול יותר לקבלת התקף לב ושבץ.
גורם
עריכה- תסמונת השחלות הפוליציסטיות
- תסמונת השחלה הפוליציסטית (PCOS) היא הפרעה אנדוקרינית המאופיינת בעודף אנדרוגנים המיוצרים על ידי השחלות. ההערכה היא שכ־90 אחוז מהנשים עם PCOS מפגינות יתר על רקע ההורמונים הללו. לא ידוע כרגע גורם קונקרטי למצב זה. הספקולציות כוללות נטייה גנטית, אם כי טרם זוהה הגן או הגנים הגורמים לתופעה הנ"ל. עדויות מצביעות על כך שהמצב עשוי להיות תורשתי. סיבות אפשריות נוספות כוללות את ההשפעות כתוצאה מגידול בייצור האינסולין. האינסולין עצמו נצפה מסוגל לגרום לעודף רמות טסטוסטרון בשחלות. ריכוז האינסולין המוגבר בגוף מביא לייצור נמוך יותר של גלובולין המחייב הורמוני מין (SHBG), גליקופרוטאין רגולטורי המדכא את תפקודם של אנדרוגנים. רמות אינסולין גבוהות בדם פועלות גם יחד עם רגישות השחלות לאינסולין וגורמות להיפר-אנדרוגנמיה, הסימפטום העיקרי של PCOS. אנשים שמנים עשויים להיות נוטים יותר לביולוגיה להציג PCOS בגלל כמויות גבוהות יותר של אינסולין בגופם. חוסר איזון הורמונלי זה יכול להוביל לחיסול כרוני, בו השחלות מתקשות לשחרר ביציות בוגרות. מקרים אלה של תפקוד לביוץ קשורים לפוריות ופרעות במחזור החודשי.
- תסמונת קושינג
- תסמונת מתפתחת כתוצאה מחשיפה ארוכת טווח להורמון קורטיזול. תסמונת קושינג יכולה להיות אקסוגנית או אנדוגנית, תלוי אם היא נגרמת על ידי מקור חיצוני או פנימי, בהתאמה. צריכת גלוקוקורטיקואידים, שהם סוג של הורמון סטרואידים, היא גורם שכיח להתפתחות תסמונת קושינג אקסוגנית. תסמונת הכריתה האנדוגנית יכולה להתרחש כאשר הגוף מייצר כמויות מופרזות של קורטיזול. מצב זה מתרחש כאשר ההיפותלמוס של המוח מעביר הורמון משחרר קורטיקוטרופין (CRH) לבלוטת יותרת המוח, אשר בתורו מפריש את הורמון האדרנוקורטיקוטרופין (ACTH). לאחר מכן, ACTH גורם לבלוטת יותרת הכליה לשחרר את הקורטיזול לדם. הסימנים לתסמונת קושינג כוללים חולשת שרירים, שטפי דם קלים, עלייה במשקל, צמיחת שיער כמו אצל זכר, סימני מתיחה צבעוניים וגוון עור אדמדם במיוחד בפנים. תסמונת קושינג הוכחה כגורמת לעודף אנדרוגן, הקושר אותה ישירות לסימנים והתסמינים הנראים בהיפר-אנדרוגניזם.
- היפרפלזיה מולדת של יותרת הכליה
- היפרפלזיה מולדת יותרת הכליה מורכבת מקבוצה של הפרעות רצסיביות אוטוזומליות הגורמות למחסור באנזים הדרוש לייצור קורטיזול ו / או אלדוסטרון, שניהם הורמונים סטרואידים. מרבית המקרים נובעים ממחסור באנזים שמשמש את הגוף לייצור קורטיזול ו-אלדוסטרון. אצל נקבות זה גורם לאי וודאות באיברי המין בלידה ובהמשך גיל ההתבגרות שיער ערווה מוגזם, הגדלת הדגדגן וצמיחה מהירה של הגוף. התסמינים אצל גברים כוללים הופעות מוקדמות של שיער הערווה, הגדלת איבר המין וצמיחה מהירה של גוף ושלד.
- גידולים
- קרצינומה אדרנוקורטיקלית הם מחלות נדירות ביותר עם שכיחות של 1–2 למיליון בשנה. מחלה זו גורמת להיווצרות תאים סרטניים בקליפת המוח של אחת או יותר משתי בלוטות יותרת הכליה. גידולים אדרנוקורטיקליים מייצרים מספר נוסף של הורמונים, ולעיתים קרובות מובילים חולים עם גידולים המייצרים הורמונים סטרואידים לפתח תסמונת קושינג, תסמונת קון והיפר-אדרוגניזם. אדנומה של בלוטת יותרת הכליה אדנומות הן גידולים שפירים בבלוטת יותרת הכליה. ברוב המקרים הגידולים אינם מראים תסמינים ואינם דורשים טיפול. עם זאת, במקרים נדירים, ייתכן וכמה אדרנומות באדרנל יופעלו, מכיוון שהן מתחילות לייצר הורמונים בכמויות גדולות בהרבה ממה שבלוטות יותרת הכליה נוטות לייצר, מה שמוביל למספר סיבוכים בריאותיים כולל אלדוסטרוניזם ראשוני והיפרנדרוגניזם.
Arrhenoblastoma
עריכהArrhenoblastoma הוא גידול נדיר בשחלה. לעיתים קרובות הוא מורכב מתאי סטרול, תאי ליידיג או שילוב כלשהו של השניים. הגידול יכול לייצר הורמונים זכריים או נשיים אצל המטופל. אצל ילד, גידול עלול לגרום לבגרות מינית מוקדמת. Arrhenoblastoma ממאיר אחראי ל-30% מכל המקרים של arrhenoblastoma, כאשר 70% האחרים הם בעיקר שפירים וניתנים לריפוי במהלך הניתוח.
- גידול על שם קרוקנברג
- גידול ממאיר המתפתח במהירות ונמצא בדרך כלל באחת מהשחלות או בשתיהן. הגידול נגרם כתוצאה מההתפשטות הטרנסקלואומית. הוא צומח בעיקר באזור הקיבה והמעי.
- גיל המעבר
- גורם אחד כזה הוא סוף הביוץ ותחילת גיל המעבר. כאשר הגוף עובר מביוץ לגיל המעבר, הוא מפסיק לשחרר אסטרוגן בקצב מהיר יותר מכפי שהוא מפסיק לשחרר אנדרוגנים. במקרים מסוימים, רמות האסטרוגן יכולות לרדת מספיק כדי שיהיו רמות גבוהות יותר של אנדרוגן המובילות להיפר-אנדרוגניזם. ירידה ברמות הורמוני המין בעוד שמדד האנדרוגן החופשי עולה, עוזרת גם לתהליך זה.
- סמים
- תסמינים הנחשבים בדרך כלל להיפראנדוגניים יכולים להתבטא גם כתוצאה של צריכת תרופות מסוימות. זה יכול לקרות על פי אחד מחמישה מנגנונים עיקריים, כלומר החדרה ישירה של אנדרוגנים לגוף, קשירת התרופה לקולטני אנדרוגן והשתתפות לאחר מכן בפעולה אנדרוגנית הפחתה של ריכוז פלזמה גלובולין-מחייב הורמון מין המביא לעלייה כתוצאה של טסטוסטרון חופשי, הפרעה ושינוי ציר ההיפותלמוס-יותרת המוח-שחלות, או לעלייה בשחרור אנדרוגנים באדרנל.
- תורשה
- מכיוון שהיפר-אנדרוגניזם יכול להופיע כסימפטום של מצבים גנטיים ורפואיים שונים, קשה להצהיר באופן כללי אם ניתן להעביר תסמינים היפר-אנדרוגניים מהורה לצאצא. עם זאת, אוסף של מצבים עם תסמינים היפר-אנדרוגניים, כולל תסמונת השחלה הפוליציסטית, נצפתה כתורשתית במקרים מסוימים. גורם פוטנציאלי אחד לתסמונת השחלה הפוליציסטית הוא היפר-אנדרוגניזם אימהי, כאשר אי סדרים הורמונליים של האם יכולים להשפיע על התפתחות הילד במהלך ההיריון, וכתוצאה מכך עוברים תסמונת השחלה הפוליציסטית מאם לילד.
אבחון
עריכהמטופלות עשויות להראות סימפטומים של היפראנדרוגניזם כבר בגילי הילדות המוקדמים, אך רופאים נוטים לפתח חשדות בעיקר כאשר המטופלת נמצאת בשלבי סיום גיל ההתבגרות ואילך.[5]
היפראנדרוגניזם לרוב מאובחן על ידי בדיקת סימנים של הירסוטיזם באמצעות מתודה סטנדרטית אשר מצביעה על הטווח של צמיחת שיער עודפת.[5][6]
בדיקת ההיסטוריה הרפואית של המטופלת ובדיקה גופנית של סימפטומים אלו הם אמצעים שמשתמשים בהם לדיאגנוזה ראשונית.[5]הערכת ההיסטוריה הרפואית של המטופלת כוללת בדיקה של גיל התרחבות בלוטות החלב (בלועזית Thelarche), גיל האדרנרכה (Adrenarche), גיל קבלת הוסת הראשון (בלועזית Menarche); דפוסים של וסת (בלועזית menstruation); השמנת יתר (בלועזית obesity) ; היסטורית הרבייה; ושל תחילתם והתפתחותם של הסימפטומים להיפראנדרוגניזם.[5] דפוסי וסת נבדקים מפני שדפוסים חריגים עלולים להופיע יחד עם הירסוטיזם.[6] היסטוריה משפחתית נבדקת גם היא במטרה לאתר הופעת סימפטומים של היפרנאדרוגניזם או של השמנת יתר בקרב בני משפחה אחרים.[5]
ניתן לבצע גם בדיקת מעבדה על מנת להעריך רמות של FSH, LH, פרולקטין, DHEAS, 17OHP, וכן רמת טסטוסטרון כוללת וחופשית בדם של המטופלת.[5] רמות גבוהות באופן חריג של כל אחד מהורמונים אלו (יחד ולחוד) מסייעות בדיאגנוזה של היפראנדרוגניזם.[5]
מניעה
עריכההיות שגורמי סיכון אינם ידועים ומשתנים בקרב מטופלים שונים, לא קיימת שיטה וודאית למניעת היפראנדרוגניזם.[7] לפיכך, תחילה נדרשים מחקרים לטווח הארוך על מנת לאתר את הגורמים למחלה לפני שבכלל ניתן יהיה למצוא דרכי מניעה מספקות.[7]
עם זאת, ישנם דברים שיכולים לעזור למנוע השלכות רפואיות ארוכות טווח הקשורות להיפראנדרוגניזם, כגון שחלות פוליציסטיות (PCOS). בדיקה על ידי רופא מומחה עבור היפראנדרוגניזם; בייחוד אם למטופלת ישנה היסטוריה משפחתית של המחלה, מחזור בלתי סדיר או סוכרת (בלועזית Diabetes); עשויה להיות מועילה.[8]הקפדה על משקל תקין ועל תזונה סדירה חשובים גם הם להפחתת הסיכויים לסיבוכים של המחלה, במיוחד בקרב נשים הסובלות מהשמנת יתר, היות שאימון גופני מתמשך והקפדה על תפריט תזונתי בריא תורמים לשיפור המחזור החודשי וכמו כן להפחתת רמות אינסולין בדם ולהפחתת ריכוזי אנדרוגן.[7]
טיפול
עריכההטיפול בהיפראנדרוגניזם משתנה בהתאם למצב הרפואי שגורם לו. בתור סימפטום הורמונלי של שחלות פוליציסטיות, גיל המעבר (בלועזית menopause), ובעיות אנדוקריניות אחרות, היפראנדרוגניזם מטופל בעיקר בתור סימפטום של בעיות אלו. באופן שיטתי, ניתן טיפול על ידי אנטי-אנדרוגנים כגון ציפרוטרון אצטט, פלוטמיד וספירונולקטון על מנת לווסת את רמון האנדרוגן בגוף המטופלת. עבור היפראנדרוגניזם הנגרם כתוצאה מהיפרפלזיה מולדת של האדרנל בהופעתה המאוחרת (בלועזית (Late-Onset Congenital Adrenal Hyperplasia (CAH), הטיפול הניתן מתמקד בעיקר על מתן הורמונים גלוקוקורטיקואידים על מנת להילחם בייצור הקורטיזול הנמוך ובייצור המוגבר של האנדרוגנים שנגרם בעקבות הנפיחות של בלוטות יותר הכליה.[9][10] גלולת מבוססות אסטרוגן ניתנות לטיפול בהיפראנדרוגניזם הנגרם הן מ-CAH והן מ-PCOS. נמצא כי טיפולים הורמונליים אלו מורידים את רמות האנדרוגן העודפות, מדכאים ייצור אנדרוגן בבלוטות יותרת הכליה ומביאים לירידה ניכרת בהירסוטיזם.[11][12]
פעמים רבות מתמודדים עם היפראנדרוגניזם באופן סימפטומטי. הירסוטיזם ואקנה מגיבים טוב לטיפולים ההורמונליים שתוארו לעיל, כאשר 60-100% מהמטופלות מדווחות על שיפור בהירסוטיזם.[11] לעומת זאת, התקרחות אנדרוגנית (בלועזית Androgenic alopecia) אינה מראה שיפור משמעותי לאור מתן טיפולים הורמונליים ולפיכך מצריכה טיפולים אחרים, כגון השתלת שיער.[13]
חברה ותרבות
עריכהכיוון שעודף אנדרוגן מתבטא במאפיינים גופניים בולטים (למשל הירסוטיזם), פעמים רבות נקשרות להיפראנדרוגניזם סטיגמות חברתיות שונות. בעולם הספורט נרשמו מקרים רבים בהם ספורטאיות נפסלו מלהתחרות מפני שרמת הטסטוסטרון שלהן הייתה גבוהה מדי.
ספורט
עריכהבעקבות המקרה של האתלטית הדרום אפריקנית קסטר סמניה, התאחדות האתלטיקה הבינלאומית (IAAF) הנהיגה מדיניות חדשה על פיה יאסר על נשים ספורטאיות להתחרות כנשים אם יש להן היפראנדרוגניזם. הבסיס להחלטה זאת הוא שלנשים אלו עשוי להיות יתרון בלתי הוגן על יריבותן.[14] החוקים קובעים כי נשים אלו יוכלו להתחרות בקטגוריית הגברים אם התוצאות שלהן יאפשרו להן.[15] ה IAAF מציין כי טסטוסטרון מקושר למסת גוף רזה, ובכך משפיע על הכוח, המהירות והכוח המתפרץ של האתלט.[16] הסף של הטסטוסטרון מעליו לא יורשה לנשים להתחרות במקצי הנשים נקבע על 10 ננומול/ליטר, בהתבסס על מחקר שבדק אתלטיות שהתחרו באליפויות העולם באתלטיקה ב 2011 ו 2013. ל 99% מהאתלטיות במחקר היו רמות טסטסטורון נמוכות מ 3.08 ננומול/ליטר.[17] במחקר שפורסם ב 2014, וסקר פרופילים אנדוקריניים של 693 ספורטאים וספורטאיות עלית, נמצא כי רק ל 13.7% מהנשים היו רמות גבוהות של טסטסטורון, בעוד של 16.5% מהגברים היו רמות טסטסטורון נמוכות.[18] עורכי המחקר ציינו כי "הייתה חפיפה מושלמת בין הטווחים של הריכוזים [בין המינים]. וזה מדגים שההחלטה של הוועד האולימפי הבינלאומי (IOC) וה IAAF להגביל השתתפות של ספורטאיות במקצי עילית רק למשתתפות עם רמות טסטסטורון "נורמליות" אינה יישומית".
תהליך בדיקת המין של נשים הוא שנוי במחלוקת, וישנן טענות כי הוא משפיל ועשוי להוביל לאפליה.[19] קיימות עדויות כי נשים ממדינות מתפתחות עברו הליכים של קליטורדקטומיות וגונדקטומיות בעקבות אבחנה של היפראנדרוגניזם.[20] בספטמבר 2014, דיוטה צ'אנד, אצנית הודית שנאסר עליה להתחרות בנשים במסגרת תחרויות של ה-IAAF, הגישה עתירה במטרה לערער על ההחלטה, מתוך רצון לחזור ולהתחרות.[21] ביולי 2015, בית המשפט לבוררות בספורט, השעה את החלטת ה-IAAF להרחיק את צ'אנד, ואפשר לה לחזור להתחרות. ל-IAAF ניתנו שנתיים במהלכן נציגי הארגון צריכים להציג ראיות מדעיות התומכות בהרחקה. בהיעדר ראיות ההרחקה תבוטל.[22][23]
השעיית בדיקות ההיפראנדרוגניזם של ה-IAAF הובילה למחלוקת במשחקים האולימפיים בריו 2016. המחלוקת באה לידי ביטוי בעיקר בנושא השתתפותה, וזכייתה במדליית הזהב בריצת 800 המטרים, של הרצה הדרום אפריקאית קסטר סמניה.[24] מתחרותיה של קסטר, לינסי שארפ וג'ואנה ג'וז'וויק, הצהירו כי הן מאמינות שלקסטר יש יתרון תחרותי בלתי הוגן.[25] במדליית הכסף, באותה תחרות, זכתה הרצה מבורונדי - פרנסין ניונסבה, שב 2019 אישרה בראיון כי גם לה יש היפראנדרוגניזם.[26] חוקרים מתחום הביו-אתיקה ותומכי שוויון מגדרי טוענים כי מניעה של השתתפות בתחרויות ספורט מנשים עם רמת טסטוסטרון גבוהה היא למעשה אפליה, בה הספורטאית "נענשת" עקב תכונה גופנית טבעית לחלוטין. הדבר דומה ליתרון טבעי של שחקן כדורסל גבוה או זורק דיסקוס עם מוטת ידיים גדולה.[27]
הגדרה חברתית
עריכהמלבד הגדרות ביוכימיות או קליניות, הגדרות תרבותיות מקובלות עשויות לקבוע את גבולות ההיפראנדרוגניזם בחברה. גדילה של שיער מעבר לרמה מסוימת ובאזורי גוף מסוימת נחשבים כטאבו בחברות מערביות רבות, גם אם מבחינה קלינית הדבר נחשב כנורמלי (למשל על פי סולם פרימן-גאלווי). לדוגמה, רק שיער ערווה ובית שחי מקובל בנשים בצפון אמריקה, בעוד ששיער באזור השפה העליונה, ה"הקו הלבן" (Linea Alba) בבטן, אזור הירכיים ומסביב לאזור הפטמה בשד אינו מקובל.[28]
ארגונים
עריכהארגונים מקצועיים כמו "Androgen Excess and PCOS Society" הוקמו על מנת לקדם את המחקר, האבחון, הטיפול והמניעה של היפראנדרוגניזם ותסמונת השחלות הפוליציסטיות, כמו גם החינוך של הציבור והקהילה המדעית אודות מצבים אלו.[29]
ראו גם
עריכהקישורים חיצוניים
עריכההערות שוליים
עריכה- ^ Bulent O. Yildiz, Diagnosis of hyperandrogenism: clinical criteria, Best Practice & Research. Clinical Endocrinology & Metabolism 20, 2006-06, עמ' 167–176 doi: 10.1016/j.beem.2006.02.004
- ^ Nora Brettenthaler, Christian De Geyter, Peter R. Huber, Ulrich Keller, Effect of the insulin sensitizer pioglitazone on insulin resistance, hyperandrogenism, and ovulatory dysfunction in women with polycystic ovary syndrome, The Journal of Clinical Endocrinology and Metabolism 89, 2004-08, עמ' 3835–3840 doi: 10.1210/jc.2003-031737
- ^ Androgen, HealthyWomen (באנגלית)
- ^ H. G. Pope, E. M. Kouri, J. I. Hudson, Effects of supraphysiologic doses of testosterone on mood and aggression in normal men: a randomized controlled trial, Archives of General Psychiatry 57, 2000-02, עמ' 133–140; discussion 155–156 doi: 10.1001/archpsyc.57.2.133
- ^ 1 2 3 4 5 6 7 Goodman, Neil, American association of clinical endocrinologists medical guidelines for clinical practice for the diagnosis and treatment of hyperandrogenic disorders, p.121, 2001
- ^ 1 2 Bulent O. Yildiz, Diagnosis of hyperandrogenism: clinical criteria, Best Practice & Research Clinical Endocrinology & Metabolism, Polycystic Ovary Syndrome and Hyperandrogenism 20, 2006-06-01, עמ' 167–176 doi: 10.1016/j.beem.2006.02.004
- ^ 1 2 3 Dan Apter, How possible is the prevention of polycystic ovary syndrome development in adolescent patients with early onset of hyperandrogenism, Journal of Endocrinological Investigation 21, 1998-10-01, עמ' 613–617 doi: 10.1007/BF03350786
- ^ Shahla Nader, Hyperandrogenism during puberty in the development of polycystic ovary syndrome, Fertility and Sterility 100, 2013-07-01, עמ' 39–42 doi: 10.1016/j.fertnstert.2013.03.013
- ^ I. A. Hughes, Management of congenital adrenal hyperplasia., Archives of Disease in Childhood 63, 1988-11-01, עמ' 1399–1404 doi: 10.1136/adc.63.11.1399
- ^ Deborah P. Merke, Stefan R. Bornstein, Congenital adrenal hyperplasia, The Lancet 365, 2005-06-18, עמ' 2125–2136 doi: 10.1016/S0140-6736(05)66736-0
- ^ 1 2 Ronald T. Burkman, The Role of Oral Contraceptives in the Treatment of Hyperandrogenic Disorders, The American Journal of Medicine 98, 1995-01-16, עמ' S130–S136 doi: 10.1016/S0002-9343(99)80071-0
- ^ George Mastorakos, Carolina Koliopoulos, George Creatsas, Androgen and lipid profiles in adolescents with polycystic ovary syndrome who were treated with two forms of combined oral contraceptives, Fertility and Sterility 77, 2002-05-01, עמ' 919–927 doi: 10.1016/S0015-0282(02)02993-X
- ^ R. Sinclair, M. Wewerinke, D. Jolley, Treatment of female pattern hair loss with oral antiandrogens, British Journal of Dermatology 152, 2005, עמ' 466–473 doi: 10.1111/j.1365-2133.2005.06218.x
- ^ STANDARD OPERATIVE PROCEDURE to identify Circumstances (Female Hyperandrogenism) in Which A Particular Sports Person will not be eligible to participate in Competitions in the Female Category, pib.gov.in
- ^ [https://stillmed.olympic.org/Documents/Commissions_PDFfiles/Medical_commission/2015-11_ioc_consensus_meeting_on_sex_reassignment_and_hyperandrogenism-en.pdf IOC Consensus Meeting on Sex Reassignment and Hyperandrogenism November 2015]
- ^ Samantha Michaels, The biggest issue in women’s sports is about to come to a head, Mother Jones (באנגלית)
- ^ Ross Tucker, The Science of Sport, Hyperandrogenism and women vs women vs men in sport: A Q&A with Joanna Harper, The Science of Sport, 2016-05-23 (באנגלית)
- ^ M. L. Healy, J. Gibney, C. Pentecost, M. J. Wheeler, Endocrine profiles in 693 elite athletes in the postcompetition setting, Clinical Endocrinology 81, 2014-08, עמ' 294–305 doi: 10.1111/cen.12445
- ^ The Humiliating Practice of Sex Testing Female Athletes - The New York Times, web.archive.org, 2016-06-28
- ^ Rebecca M. Jordan-Young, Peter H. Sönksen, Katrina Karkazis, Sex, health, and athletes, BMJ (Clinical research ed.) 348, 2014-04-28, עמ' g2926 doi: 10.1136/bmj.g2926
- ^ Macur, Juliet (2014-10-06). "Fighting for the Body She Was Born With". The New York Times (באנגלית אמריקאית). ISSN 0362-4331. נבדק ב-2019-12-24.
- ^ Branch, John (2015-07-27). "Dutee Chand, Female Sprinter With High Testosterone Level, Wins Right to Compete". The New York Times (באנגלית אמריקאית). ISSN 0362-4331. נבדק ב-2019-12-24.
- ^ "Dutee Chand cleared to race as IAAF suspends 'gender test' rules" (באנגלית בריטית). 2015-07-27. נבדק ב-2019-12-24.
- ^ Caster Semenya’s Olympic dream a topic of controversy, Orange County Register, 2016-07-31 (באנגלית)
- ^ Fifth-placed runner behind Semenya 'feels like silver medalist' and glad she was the 'second white', The Independent, 2016-08-22 (באנגלית)
- ^ Ken Goe | The Oregonian/OregonLive, Francine Niyonsaba of OTC Elite opens up, and good for her: Oregon track & field rundown, oregonlive, 2019-04-17 (באנגלית)
- ^ Longman, Jeré (2016-08-18). "Understanding the Controversy Over Caster Semenya". The New York Times (באנגלית אמריקאית). ISSN 0362-4331. נבדק ב-2019-12-24.
- ^ Krishna, Usha R, Adolescent Gynecology (pb), Orient Blackswan, 2000. (באנגלית)
- ^ Androgen Excess and PCOS Society, www.ae-society.org
הבהרה: המידע בוויקיפדיה נועד להעשרה בלבד ואינו מהווה ייעוץ רפואי.