אבולוציה של יוני מתכת במערכות ביולוגיות
האבולוציה של יוני מתכת במערכות ביולוגיות עוסקת בהתפתחות תהליכי חדירת יוני מתכת שונים לתאי בעלי חיים וקשירתם לחלבוני התא, למשל אנזימים ונשאי מתכות. היא עוסקת גם בשינויים האבולוציוניים של חילוף החומרים במערכות ביולוגיות שונות בעקבות חדירה זו. מתכות אלה מכונות ביו-מתכות (אנ')[1] והן כוללות ריכוזים גבוהים של יוני המתכות ברזל, מנגן, מגנזיום, אבץ, וריכוזים נמוכים יחסית של נחושת, קובלט, ניקל, סלניום, מוליבדן, כרום וטונגסטן.[2]
המתכות נקשרות לחלבוני תא המכונים מטאלופרוטאינים באתרים נקודתיים ועל ידי כך מייעלות את זיקתם של החלבונים למצעים שונים (סובסטרטים). 30% מחלבוני התא הם חלבונים קושרי מתכות. תפקיד המתכות לשמש כקואנזימים המזרזים את הפעילות האנזימטית התוך-תאית באופן משמעותי בהשוואה לראקציות נטולות מתכות.[3] מעל ל-40% מן הראקציות האנזימטיות מערבות יוני מתכת.[4] תפקיד נוסף של מטלופרוטאינים הוא שינוע ברזל ונחושת באמצעות הנסיוב.[5]
חשיפת יתר למתכות עלולה להוביל לתופעות של רעילות. חדירת המתכות לתאים והוצאת כמויות עודפות מן התאים מתבצעת על ידי מערכות אנזימטיות מורכבות. במהלך האבולוציה נוצר איזון בין האנזימים המייבאים את המתכות אל התאים, לבין אלה המייצאים את המתכות מן התאים לסביבה החיצונית, כמו גם תהליכים של הסתגלות התאים למתכות השונות.[6]
תקופת האטמוספירה הפרביוטית
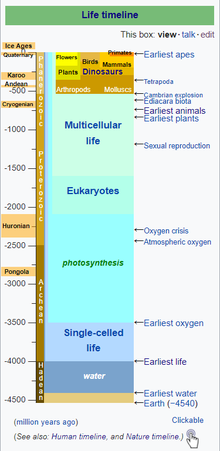
עריכההתקופה הפרביוטית נחשבת לתקופה האבולוציונית השנייה של כדור הארץ.[7] בתקופה זו, לפני 4 מיליארד שנים, שררו על פני כדור הארץ תנאים של חוסר חמצן. האטמוספירה (אנ') הייתה מורכבת מפחמן דו-חמצני, חנקן, וכמויות מזעריות של גזים מחזרים: מתאן, אמוניה ומימן וכמויות אפסיות של חמצן.[8]
השערת עולם ה-RNA
עריכה- ערך מורחב – השערת עולם ה-RNA
על פי התאוריה של "עולם ה־RNA" שהתפתחה בשנים המאוחרות של המאה העשרים על ידי מרק נבה ושותפיו[9] חומצות הגרעין מקבוצת ה-RNA הופיעו ראשונות ביקום, לפני הופעת ה-DNA ולפני החלבונים. לפי השערה זו, מולקולות ה-RNA נוצרו ראשונות וקדמו לפפטידים קושרי-המתכות.[10] הפפטידים הראשונים המוגדרים כשרשראות קצרות של חומצות אמינו היו מעורבים בקשירת מתכות ובהולכת אלקטרונים קדמו לחלבונים הקדמוניים שהם שרשראות ארוכות יותר של חומצות אמינו. קשרים אלה נוצרו לפני יותר מ-3.8 מיליארד שנים.[11] הפפטידים בעלי היכולת לקשור מתכות וה-RNA הובילו להתפתחות חלבונים מורכבים יותר.[12]
התהוות המטלופרוטאינים
עריכה- ערך מורחב – מטאלופרוטאין
ראשית החיים קשורה ליכולת של מקטעי חלבונים ראשוניים ליצור קשרים כימיים עם מתכות. המפגש בין החלבונים למתכות התאפשר לפני כמעט 4 מיליארד שנים בסביבה המכונה "המרק הקדום", סביבה מימית, עשירה במולקולות אורגניות ומינרלים הניחה את התשתית להיווצרות חלבונים רבים. חוקרים טוענים שהתרכובות הקדומות האלה אפשרו את התפתחותם של החלבונים האחראים להובלת אלקטרונים בין אטומים שהפך לתהליך חיוני לקיומם של החיים עצמם. בתקופה הפרביוטית, הקרקע על פני כדור הארץ הייתה עשירה במימן גופרי. הסביבה החומצית של "המרק הקדום" אפשרה המסה של רבה יותר של ברזל בהשוואה למתכות אחרות וקשירת יוני הברזל לחלבונים, בהתאם למודל של Irving–Williams series (אנ') בסביבה המחזרת ששרתה בתקופה הפרביוטית ויצירת מולקולות של חד-תחמוצת-הפחמן מדו-תחמוצת-הפחמן ויצירת הידרוציאניד מחנקן אטמוספירי, התאפשרה הודות למתכות המעבר.[13]
האטמוספירה ב"אסון החמצן"
עריכהלפני 2.4 מיליארדי שנים החל תהליך של פליטת חמצן לאטמוספירה של כדור הארץ בתקופה המכונה "אסון החמצן" הקרוי גם "אירוע החמצן הגדול".[14] תקופה זו קרתה בעקבות התפתחות חיידקי ציאנובקטריה[15] בעלי יכולת לבצע פוטוסינתזה. העשרת האטמוספירה בחמצן הובילה לזירוז חמצון הגופרית לגופרות ולתחמוצת הגופרית. כתוצאה מכך חל זירוז המסת המתכות אבץ, נחושת, ניקל וקובלט על ידי הפיכתן לתחמוצות במי "המרק הקדום"[16] והעלאת זמינותן למערכות הביולוגיות של התאים.[17]
האבולוציה של קשירת המתכות לחלבוני התא
עריכהחיוניות המתכות לתהליכים המטבוליים של התא מחיבת מנגנוני קשירה ואגירה במערכות תוך-תאיות. תהליך זה מבטיח זמינות לאורך זמן. מחקרים שנעשו בחלבונים קושרי המתכות ברזל, נחושת וניקל התמקדו באתרים המצויים בהם. באתרים אלה זוהתה קבוצה קטנה של פפטידים בעלי מבנה דומה, על אף השוני של החלבונים עצמם. נמצא שאתרים קושרי מתכות מורכבים לרוב מיחידות מבניות קטנות החוזרות על עצמן. אותן אבני בניין נמצאו גם באזורים אחרים בחלבונים ולא רק באזורים קושרי מתכות ובחלבונים רבים נוספים. על סמך ניתוח המבנה של פפטידים שהתגלו כאופייניים לאזורים קושרי מתכות בחלבון, הסיקו החוקרים שהפעילות הביולוגית הראשונה של חלבונים הייתה כנראה הולכת אלקטרונים על ידי אותם הפפטידים קושרי המתכות.[18]
שאר התפקידים שהחלבונים ממלאים בתא החי התפתחו בשלבים מאוחרים יותר.[18][19] יונים של מתכות מצויים ברקמות של בעלי-חיים וממלאים תפקידים מגוונים במערכות ביולוגיות.[20] חלקם הגדול משתייך לקבוצת מתכות המעבר בטבלה המחזורית, כגון, מגנזיום, מנגן, ברזל, אבץ, נחושות, ניקל וקובלט. המטלואנזימים מעורבים במחזוריות האלמנטים בטבע.[21]
מגנזיום
עריכהמגנזיום מצוי בשפע בעולם החי והצומח כקטיון דו-ערכי, בעיקר בציטופלזמה, בעצמות ובכלורופלסטים, מיעוטו נמצא גם בנסיוב.[22] ברקמות הוא מצוי בצורת מגנזיום-ATP,[23] כאחראי על מעברי האנרגיה[24] ומשמש כקו-פקטור ל-300 אנזימים האחראים על מגוון רחב של פעילויות ביוכימיות[25] ברקמות החי והצומח. למגנזיום חשיבות רבה בתהליכים הביולוגיים של האורגניזם: פעילות שרירים ועצבים, ויסות לחץ הדם, ויסות ריכוז הגלוקוז בדם, סינתזה של חלבונים, גלוטטיון, DNA ו-RNA ובתהליכי הפקת אנרגיה בפוספורילציה אוקסידטיבית וגליקוליזה.[26] יוני המגנזיום אחראים על ויסות המעבר הפעיל של יוני סידן ואשלגן בקרומי התא, בעל תפקיד מרכזי בתהליכי בניית השלד[27] ואחראי על קצב פעילות הלב.[28] באורגניזמים השייכים לפרוקריוטה ובצמחים המסוגלים לבצע פוטוסינתזה המגנזיום הוא יון מרכזי במבנה הכלורופיל, פיגמנט המאורגן בטילקואידים (tylokoid) המצויים בכלורפלסטים.[29]
מנגן
עריכההמנגן כקטיון דו-ערכי הוא קו-פקטור חשוב בתהליכי הפוטוסינתזה. ההשערה היא שכבר בתחילת האבולוציה של תהליכי הפוטוסינתזה כשהאטמוספירה הייתה נטולת חמצן, יוני המנגן היוו מקור לאלקטרונים. בשלב התחלתי זה, התפתחה היכולת לנצל את אנרגיית השמש ליצירת חומרים אורגניים אשר היוו נידבך ביצירת אורגניזמים קדומים שקדמו לציאנובקטריה. בשלב האבולוציוני הבא התפתחו בחיידקי הציאנובקטריה מבנים המכונים תילקואידים, שהם מרכזים אנרגטיים לביצוע תהליכי הפוטוסינתזה. תהליך זה הוביל להעשרת האטמוספירה בחמצן. האווירה על פני כדור הארץ הפכה מאל-אווירנית לאווירנית.[30] היצורים הפרוקריוטים, נושאי הטילקואידים נבלעו על ידי יצורים אאוקריוטים בתהליכי אנדוסימביוזה. האנדוסימביוזה אפשרה את העברת תהליך הפוטוסינתזה מיצורים פרוקריוטים פשוטים ליצורים אאוקריוטים מורכבים, כגון אצות וצמחים מפותחים. המנגן המשמש כקו-פקטור באנזימים רבים ניתן להחלפה על ידי קטיונים דו-ערכיים אחרים, כגון, סידן, קובלט, נחושת, מגנזיום או אבץ. אולם, בתהליך הפוטוסינתזה, יוני המנגן המיצרים את הקומפלקס (Mn4O5Ca)אינם ניתנים להחלפה על ידי מתכות אחרות.[31]
תהליך הפוטוסינתזה שבו משתחררות מולקולות של חמצן גרם להופעת אורגניזמים המכונים ROS (Reactive oxygen species),[32] בעלי מנגנונים אנזימטיים המנטרלים את האפקט הרעיל של המטבוליטים: מימן על-חמצני, על-תחמוצת ורדיקל הידרוקסיל (Hydroxyl radical) הנחשב לרדיקל חופשי. המנגן הוא קו-פקטור לאנזימים Mn-Dismutase[33] וקטאלז[34] הממוקמים בכלורופלסטים, במיטוכונדריה בפראוקסיזומים ובקרום התא. אברונים אלה התפתחו בשלבים המוקדמים של אבולוציית התאים.[35]
אנזימים אלה מנטרלים תוצרים רעילים הנוצרים בתהליכים המטבוליים של התא ועל ידי כך מנטרלים את היכולת לגרום לנזקים בלתי הפיכים למרכיבי תא חיוניים על ידי פגיעה בחלבונים, בחומצות הגרעין ובליפידים ותמותת תאים.[36][37][38]
ברזל
עריכההברזל נחשב לאחת המתכות החשובות ביותר לתהליכים המטבוליים התאיים. הברזל הוא קו-פקטור עיקרי בכל שלבי הנשימה התאית במעבר אלקטרונים בין ברזל דו-ערכי לתלת-ערכי וההפך.[39]
הקומפלקסים של ברזל-גופרית המתקשרים לחלבונים נחשבים למטלופרוטאינים הראשונים שנוצרו בתהליכי האבולוציה של הפוטוסינתזה. הם נוצרו מהתקשרות של פפטידים עם משקעים של מלחי Fe2(SO4)3(H2O)n. הפיכת הברזל הדו-ערכי לברזל תלת-ערכי הכרחיים לתהליכים ביולוגיים ומחזור הברזל בטבע.[40]
הברזל מהווה מרכיב חשוב במערכות ביולוגיות שונות: ציטוכרומים המצויים בקרום המיטוכונדריה, הקטאלזות האחראיות לפרוק מי-חמצן, המיוגלובין כנושא החמצן העיקרי בשרירים, ההם-פראוקסידזה (Haem peroxidase) המעורב בקשירת החמצן להמוגלובין,[41] האנזים סינטאזה NOS (Endothelial NOS) האחראי ליצירת תחמוצת החנקן מארגינין, המשמש כמולקולת איתות בפרוקריוטה ואאוקריוטה,[42] והפריטין, חלבון נושא ברזל המצוי בציטופלזמה, המווסת את ריכוז הברזל בתאים ומבטיח ריכוזים נאותים באורגניזם למניעת מחסור ונזקים כתוצאה מעודף ברזל.[43]
-
מבנה סכמטי של קבוצת הם בהמוגלובין- קשירת ברזל
-
מבנה סכמטי של האנזים קטלאזה, בעל ארבע מולקולות של הם Heme
-
מבנה של קו אנזים FeMo -קשירת יוני ברזל ומוליבדן
ניקל וקובלט
עריכההניקל שריכוזו נמוך בקרקע, מהווה גורם חשוב בהתפתחות הקדומה של צורות חיים על פני כדור הארץ. הטבעת הפורפירינית בעלת יכולת לקשור את המתכות ברזל, מגנזיום, ניקל וקובלט וליצור קו-אנזימים אחראים על מגוון רחב של תהליכים אנזימטיים בתא החי. יוני המתכות ניקל וקובלט מעורבים ביצירת מטלופרוטאינים. הניקל יוצר עם טבעת הפורפירין קומפלקס הקרוי F-430, קו-אנזים מתיל רדוקטאזה (Methyl coenzyme M reductase) המשתתף בתהליך האנזימטי של שחרור גז המתאן.[44] התוצאה של קשירת הקובלט לטבעת הפורפירין היא יצירת קו-אנזים בעל חשיבות מטבולית גבוהה בשם ציאנקובלאמין (Cyancobalamine)[45] ההופך לוויטמין B12 שהוא ויטמין חיוני לגוף לתפקוד מערכת העצבים וייצור DNA.[46]
-
מבנה סכמטי של קו אנזים B12 -קשירת יוני קובלט
-
מבנה סכמטי של קו אנזים M -קשירת יוני ניקל
נחושת
עריכההנחושת ויוני הנחושת נחשבים לקשי-תמס ולכן לא היו זמינים לתאים הקדומים בראשית התהליך האבולוציוני. העשרת האטמוספירה בחמצן בתקופת "אירוע החמצן הגדול" אפשרה התמוססות נחושת אלמנטרית ויוני הנחושת החד-ערכיים והפיכתם ליונים דו-ערכיים ולהתהוות מטלופרוטאינים קושרי נחושת. מרבית האנזימים השייכים לקבוצת המטלופרוטאינים קושרי הנחושת מצויים באאוקריטה. רק מספר קטן של מטלופרוטאינים אלה נמצאים בפרוקריוטה, ציאנובקטריה וחיידקים אווירניים, דוגמת האנזים סופראוקסיד דיסמוטאז (SOD) על שלוש צורותיו: האנזימים Fe-SOD (קושר ברזל) ו-Mn-SOD (קושר מנגן) מצויים בכל הפרוקריוטה ובמיטוכונדריה של אאוקריוטה.[47]
לעומת זאת, האנזים Cu-SOD (קושר נחושת) מצוי בציטופלזמה ובכלורופלסטים של האאוקריוטיה בלבד. שלושת האנזימים מקבוצת ה-SOD מפרקים מולקולות של סופראוקסיד הנחשב לרעיל למי חמצן. אלו מתפרקים בהמשך על ידי הקטלאזה לחמצן ומים. אנזימי ה-SOD והקטלאזה שומרים על התא בפני רעילותם של רדיקלי חמצון חופשיים.[48][47] מתכות נוספות הנקשרות לחלבונים שלא באמצעות טבעת ההם הן אבץ, מוליבדן, ונדיום.[49]
אבץ
עריכההאבץ הוא מתכת שחדרה לתאים החיים בשתי תקופות אבולוציוניות. לפני 3–4 מיליארדי שנים, כאשר שררה אווירה אל-אווירנית על פני כדור הארץ, האבץ היה מצוי כאבץ גופריתי בגלל הסביבה החומצית של "הים הקדום" אשר אפשרה לאבץ להתקשר למימן הגופריתי ולהפוך לאבץ גופריתי ולהתקשר לחלבוני תאים של מיקרואורגניזמים אל-אווירניים, לפרוטאזות ונוקלאזות שהיו אנזימים חוץ-תאיים, ולסינטטאזות, ודהידרוגנאזות שהן אנזימים תוך-תאיים. בתקופת "אירוע החמצון הגדול", חל זירוז של חדירת אבץ למערכות הביולוגיות בממלכת הפרוטיסטה.[50]
לאבץ תפקיד חשוב באיזון המבנה המולקולרי של גורמי השעתוק המצויים באאוקריוטה על ידי איזון קיפולי החלבון של גורמי השעתוק באמצעות הקופקטור Sp1.[51][52]
מוליבדן
עריכהמוליבדן ויוני מוליבדן מצויים במרכזים פעילים של מטלואנזימים באורגניזמים רבים השייכים לעל-ממלכת הארכאה, על-ממלכת הבקטריה, עובשים, החי והצומח. המוליבדן הוא קו-פקטור באנזימים האחראים על תהליכי ההפיכה של פחמן, חנקן, גופרית, ארסן, סלניום וכלור בטבע, וכן של חומרים המכילים קבוצת קרבונילים, כגון אלדהידים, חד-תחמוצת-הפחמן ודו-תחמוצת-הפחמן. מוליבדן משמש כקו-אנזים באנזימים מקבוצת הניטרוגנאזות (Nitrogenase). אנזימים אלה מכילים הן מוליבדן והן ברזל ומצויים בחיידקים סימביוטים של צמחים ואחראים על קיבוע חנקן אטמוספירי והפיכתו לאמוניה המוביל לסינתזה של חלבונים. למוליבדן תפקיד חשוב גם במבנה של אנזימים המשתתפים במטבוליזם הגופרית המצויים במגוון רחב של אורגניזמים. בדומה לאבץ, המסת המוליבדן גברה בתקופת "אירוע החמצון הגדול", כאשר חלה האצה של הפיכת מוליבדן סולפיד למוליבדאט בעל מסיסות גבוהה יותר, ועל ידי כך, הגברת חדירתו לתאים וקשירתו לאנזימים התוך-תאיים. הפיכת המוליבדן לקו-אנזים בתהליך האבולוציוני גרמה להיותו מתכת הכרחית לתהליכים הביולוגיים האלה.[53]
טונגסטן
עריכהטונגסטן הוא אחת המתכות הקדומות ביותר שנקשרו למערכות ביולוגיות. בתקופה הפרביוטית. הים הקדום היה עשיר בטונגסטן וגופרית ודל במוליבדן. לכן הטונגסטן חדר למערכות חיים ימיות. החיידק (Pyrococcus furiosus) השייך לעל-ממלכת הארכאה חי במקווי מים תרמיים. זהו חיידק אל-אווירני אובליגטורי, אקסטרמופילי והטרוטרופי, המתקיים בטמפרטורות שבין 70-103oC וזקוק ליוני טונגסטן לגידולו. החיידק מכיל מספר אנזימים עמידים לחום מקבוצת הדהידרוגנאזות, מקבוצת ה-(Alcohol dehydrogenase).[55] המטלואנזימים הללו המכילים ברזל או אבץ וחמישה אנזימים מקבוצת אוקסידורדוקטזה (Oxidoreductase) מכילים ברזל, טונגסטן וגופרית.[56]
ונדיום
עריכהונדיום נחשב לאחת המתכות הקדומות ביותר שנקשרו למערכות ביולוגיות. החיידק אזוטובקטר וינלנדי (Azotobacter vinelandii) הוא מתג גראם שלילי, אווירני הקושר חנקן אטמוספירי על ידי חיזורו לאמוניה. התהליך מבוצע על ידי האנזים ניטרוגנאזה (Nitrogenase), באמצעות קו-פקטור המכיל יוני ברזל ומוליבדן. המוליבדן עשוי להיות מוחלף על ידי יוני ונדיום על פי זמינות המתכות השונות.[49] היותו של החיידק אווירני מעידה על תקופה התפתחותית בסביבת חמצן, המתאים לתקופת "אירוע החמצון הגדול" של לפני 2.4 מיליארדי שנים. הוא מקורב מבחינה גנטית לחיידק Pseudomona aeruginosa, ממשפחה פסאודומונדה.[57]
סלניום
עריכהסלניום[58] משמש כקו-פקטור באנזימים רבים של הפרוקריוטה. אתר הפעילות שלו הוא סלניום-ציסטאין. הגנים האחראים ליצירת סלנופרוטאינים מצויים הן בעל-ממלכת הארכאה והן בעל-ממלכת הבקטריה.[59]
אבולוציה של פתוגניות בחיידקים
עריכההתפתחות של פתוגניות של חיידקים מסוימים בגוף פונדקאי, תלויה בזמינותן של מתכות המאפשרות לפתח את אלימותם. במחקרים שנעשו על חיידקים שונים, כגון, Pseudomonas aeruginosa המוגדר כחיידק קומנסלי שעלול להפוך לחיידק פתוגני בתנאים מסוימים.[60] הפיכתו של החיידק לפתוגני מעודדת תחרותיות בינו לבין הפונדקאי על מתכות המעבר, ומאפשרת פיתוח יכולות לשימוש במתכת חיונית אחת במקומה של מתכת אחרת בהתאם לזמינותה במערכת.[61]
הערות שוליים
עריכה- ^ Christopher L. Dupont, Andrew Butcher, Ruben E. Valas, Philip E. Bourne, Gustavo Caetano-Anollés, History of biological metal utilization inferred through phylogenomic analysis of protein structures, Proceedings of the National Academy of Sciences 107, 2010-06-08, עמ' 10567–10572 doi: 10.1073/pnas.0912491107
- ^ Michael S. Wang, Kenric J. Hoegler, Michael H. Hecht, Unevolved De Novo Proteins Have Innate Tendencies to Bind Transition Metals, Life 9, 2019-01-09, עמ' 8 doi: 10.3390/life9010008
- ^ Metalloprotein | chemical compound | Britannica, www.britannica.com (באנגלית)
- ^ Kevin J. Zahnle, Roxana Lupu, David C. Catling, Nick Wogan, Creation and Evolution of Impact-generated Reduced Atmospheres of Early Earth, The Planetary Science Journal 1, 2020-05-01, עמ' 11 doi: 10.3847/psj/ab7e2c
- ^ Hiroshi Kawabata, Transferrin and transferrin receptors update, Free Radical Biology and Medicine 133, 2019-03, עמ' 46–54 doi: 10.1016/j.freeradbiomed.2018.06.037
- ^ Kevin J. Waldron, Nigel J. Robinson, How do bacterial cells ensure that metalloproteins get the correct metal?, Nature Reviews Microbiology 7, 2009-01, עמ' 25–35 doi: 10.1038/nrmicro2057
- ^ Sujoy Mukhopadhyay, Rita Parai, Noble Gases: A Record of Earth's Evolution and Mantle Dynamics, Annual Review of Earth and Planetary Sciences 47, 2019-05-30, עמ' 389–419 doi: 10.1146/annurev-earth-053018-060238
- ^ Kevin J. Zahnle, Roxana Lupu, David C. Catling, Nick Wogan, Creation and Evolution of Impact-generated Reduced Atmospheres of Early Earth, The Planetary Science Journal 1, 2020-06-01, עמ' 11 doi: 10.3847/PSJ/ab7e2c
- ^ Marc Neveu, Hyo-Joong Kim, Steven A. Benner, The “Strong” RNA World Hypothesis: Fifty Years Old, Astrobiology 13, 2013-04, עמ' 391–403 doi: 10.1089/ast.2012.0868
- ^ Ben K. D. Pearce, Ralph E. Pudritz, Dmitry A. Semenov, Thomas K. Henning, Origin of the RNA world: The fate of nucleobases in warm little ponds, Proceedings of the National Academy of Sciences 114, 2017-10-24, עמ' 11327–11332 doi: 10.1073/pnas.1710339114
- ^ Origin of Life: Study Reveals How Peptides Formed in the Early Earth, Inverse, 2019-07-11
- ^ G. E. Fox, Origin and Evolution of the Ribosome, Cold Spring Harbor Perspectives in Biology 2, 2010-09-01, עמ' a003483–a003483 doi: 10.1101/cshperspect.a003483
- ^ A. Lazcano, Historical Development of Origins Research, Cold Spring Harbor Perspectives in Biology 2, 2010-11-01, עמ' a002089–a002089 doi: 10.1101/cshperspect.a002089
- ^ Something went wrong..., new.huji.ac.il
- ^ William Martin, Michael J. Russell, On the origins of cells: a hypothesis for the evolutionary transitions from abiotic geochemistry to chemoautotrophic prokaryotes, and from prokaryotes to nucleated cells, Philosophical Transactions of the Royal Society of London. Series B: Biological Sciences 358, 2003-01-29, עמ' 59–85 doi: 10.1098/rstb.2002.1183
- ^ אבני הבניין של החיים, באתר מכון דוידסון לחינוך מדעי, 2020-12-02
- ^ William Martin, Michael J. Russell, On the origins of cells: a hypothesis for the evolutionary transitions from abiotic geochemistry to chemoautotrophic prokaryotes, and from prokaryotes to nucleated cells, Philosophical Transactions of the Royal Society of London. Series B: Biological Sciences 358, 2003-01-29, עמ' 59–85 doi: 10.1098/rstb.2002.1183
- ^ 1 2 Yana Bromberg, Ariel A. Aptekmann, Yannick Mahlich, Linda Cook, Stefan Senn, Maximillian Miller, Vikas Nanda, Diego U. Ferreiro, Paul G. Falkowski, Quantifying structural relationships of metal-binding sites suggests origins of biological electron transfer, Science Advances 8, 2022-01-14 doi: 10.1126/sciadv.abj3984
- ^ Encyclopedia of Inorganic and Bioinorganic Chemistry, 2, Wiley, 2012-02, ISBN 978-1-119-95143-8. (באנגלית)
- ^ Robert J. P. Williams, Systems biology of evolution: the involvement of metal ions, BioMetals 20, 2007-04-01, עמ' 107–112 doi: 10.1007/s10534-007-9087-6
- ^ Peter M. H. Kroneck, The Biogeochemical Cycles of the Elements and the Evolution of Life, CRC Press, 2005, ISBN 978-0-429-16464-4
- ^ Office of Dietary Supplements - Magnesium, ods.od.nih.gov (באנגלית)
- ^ Elisabeth Gout, Fabrice Rébeillé, Roland Douce, Richard Bligny, Interplay of Mg 2+, ADP, and ATP in the cytosol and mitochondria: Unravelling the role of Mg 2+ in cell respiration, Proceedings of the National Academy of Sciences 111, 2014-10-28 doi: 10.1073/pnas.1406251111
- ^ Definition: magnesium from Online Medical Dictionary, web.archive.org, 2007-12-25
- ^ G. Webb, Modern Nutrition in Health and Disease, 9th edition. M. E. Shils, J. A. Olsen, M. Shike and A. C. Ross (editors). 1999. Baltimore: Williams & Wilkins. $105.00. ISBN 0-683-30769-X, British Journal of Nutrition 82, 1999-10, עמ' 331–332 doi: 10.1017/s0007114599001555
- ^ Read "Dietary Reference Intakes for Calcium, Phosphorus, Magnesium, Vitamin D, and Fluoride" at NAP.edu. (באנגלית)
- ^ S Wallach, Effects of magnesium on skeletal metabolism, Magnesium and trace elements 9, 1990-01-01, עמ' 1–14
- ^ Magnesium and Heart Rate, LIVESTRONG.COM (באנגלית)
- ^ Role of Magnesium in Plant Culture | PRO-MIX Greenhouse Growing, www.pthorticulture.com
- ^ Blog, OMEX Agriculture Inc., 2020-05-21
- ^ Santiago Alejandro, Stefanie Höller, Bastian Meier, Edgar Peiter, Manganese in Plants: From Acquisition to Subcellular Allocation, Frontiers in Plant Science 11, 2020 doi: 10.3389/fpls.2020.00300/full#b17
- ^ Baishnab Charan Tripathy, Ralf Oelmüller, Reactive oxygen species generation and signaling in plants, Plant Signaling & Behavior 7, 2012-12, עמ' 1621–1633 doi: 10.4161/psb.22455
- ^ Manganese Superoxide Dismutase - an overview | ScienceDirect Topics, www.sciencedirect.com
- ^ Ankita Nandi, Liang-Jun Yan, Chandan Kumar Jana, Nilanjana Das, Role of Catalase in Oxidative Stress- and Age-Associated Degenerative Diseases, Oxidative Medicine and Cellular Longevity 2019, 2019-11-11, עמ' 1–19 doi: 10.1155/2019/9613090
- ^ Geoffrey M. Cooper, The Origin and Evolution of Cells, Sinauer Associates, 2000. (באנגלית)
- ^ Munehiro Kitada, Jing Xu, Yoshio Ogura, Itaru Monno, Daisuke Koya, Manganese Superoxide Dismutase Dysfunction and the Pathogenesis of Kidney Disease, Frontiers in Physiology 11, 2020 doi: 10.3389/fphys.2020.00755/full
- ^ Mengfan Liu, Xueyang Sun, Boya Chen, Rongchen Dai, Zhichao Xi, Hongxi Xu, Insights into Manganese Superoxide Dismutase and Human Diseases, International Journal of Molecular Sciences 23, 2022-01, עמ' 15893 doi: 10.3390/ijms232415893
- ^ Gf Gaetani, Am Ferraris, M Rolfo, R Mangerini, S Arena, Hn Kirkman, Predominant role of catalase in the disposal of hydrogen peroxide within human erythrocytes, Blood 87, 1996-02-15, עמ' 1595–1599 doi: 10.1182/blood.V87.4.1595.bloodjournal8741595
- ^ Austin D. Read, Rachel ET. Bentley, Stephen L. Archer, Kimberly J. Dunham-Snary, Mitochondrial iron–sulfur clusters: Structure, function, and an emerging role in vascular biology, Redox Biology 47, 2021-11, עמ' 102164 doi: 10.1016/j.redox.2021.102164
- ^ Kevin G. Taylor; Kurt O. Konhauser, Iron in Earth Surface Systems: A Major Player in Chemical and Biological Processes, pubs.geoscienceworld.org
- ^ Massimo Paoli, Jon Marles-Wright, Ann Smith, Structure–Function Relationships in Heme-Proteins, DNA and Cell Biology 21, 2002-04, עמ' 271–280 doi: 10.1089/104454902753759690
- ^ A Uzman, Molecular Cell Biology (4th edition) Harvey Lodish, Arnold Berk, S. Lawrence Zipursky, Paul Matsudaira, David Baltimore and James Darnell; Freeman & Co., New York, NY, 2000, 1084 pp., list price $102.25, ISBN 0-7167-3136-3, Biochemistry and Molecular Biology Education 29, 2001, עמ' 126–128 doi: 10.1016/s1470-8175(01)00023-6
- ^ Elizabeth C. Theil, FERRITIN: STRUCTURE, GENE REGULATION, AND CELLULAR FUNCTION IN ANIMALS, PLANTS, AND MICROORGANISMS, Annual Review of Biochemistry 56, 1987-06, עמ' 289–315 doi: 10.1146/annurev.bi.56.070187.001445
- ^ Juan C Fontecilla-Camps, Nickel and the origin and early evolution of life, academic.oup.com, 16 March 2022
- ^ S. Frank, A.A. Brindley, E. Deery, P. Heathcote, A.D. Lawrence, H.K. Leech, R.W. Pickersgill, M.J. Warren, Anaerobic synthesis of vitamin B12: characterization of the early steps in the pathway, Biochemical Society Transactions 33, 2005-08-01, עמ' 811–814 doi: 10.1042/bst0330811
- ^ Robert J. P. Williams, The symbiosis of metal and protein functions, European Journal of Biochemistry 150, 1985-07, עמ' 231–248 doi: 10.1111/j.1432-1033.1985.tb09013.x
- ^ 1 2 Ei-Ichiro Ochiai, Copper and the biological evolution, Biosystems 16, 1983-01, עמ' 81–86 doi: 10.1016/0303-2647(83)90029-1
- ^ Enrique Cadenas, Kelvin J.A. Davies, Mitochondrial free radical generation, oxidative stress, and aging11This article is dedicated to the memory of our dear friend, colleague, and mentor Lars Ernster (1920–1998), in gratitude for all he gave to us., Free Radical Biology and Medicine 29, 2000-08, עמ' 222–230 doi: 10.1016/S0891-5849(00)00317-8
- ^ 1 2 Oliver Einsle, Douglas C. Rees, Structural Enzymology of Nitrogenase Enzymes, Chemical Reviews 120, 2020-06-24, עמ' 4969–5004 doi: 10.1021/acs.chemrev.0c00067
- ^ R. J. P. Wiiliams, Zinc in evolution, Journal of Inorganic Biochemistry, Bert Vallee Memorial 111, 2012-06-01, עמ' 104–109 doi: 10.1016/j.jinorgbio.2012.01.004
- ^ S. S. Krishna, Structural classification of zinc fingers: SURVEY AND SUMMARY, Nucleic Acids Research 31, 2003-01-15, עמ' 532–550 doi: 10.1093/nar/gkg161
- ^ R.J.P. Wiiliams, Zinc in evolution, Journal of Inorganic Biochemistry 111, 2012-06, עמ' 104–109 doi: 10.1016/j.jinorgbio.2012.01.004
- ^ Ralf R. Mendel, Cell biology of molybdenum, BioFactors 35, 2009-09, עמ' 429–434 doi: 10.1002/biof.55
- ^ Ana-Maria Sevcenco, Martijn W. H. Pinkse, Emile Bol, Gerard C. Krijger, Hubert Th. Wolterbeek, Peter D. E. M. Verhaert, Peter-Leon Hagedoorn, Wilfred R. Hagen, The tungsten metallome of Pyrococcus furiosus, Metallomics 1, 2009, עמ' 395 doi: 10.1039/b908175e
- ^ Ronnie Machielsen, Agustinus R. Uria, Servé W. M. Kengen, John van der Oost, Production and Characterization of a Thermostable Alcohol Dehydrogenase That Belongs to the Aldo-Keto Reductase Superfamily, Applied and Environmental Microbiology 72, 2006-01, עמ' 233–238 doi: 10.1128/AEM.72.1.233-238.2006
- ^ Swarnalatha Mukund, Michael W.W. Adams, Glyceraldehyde-3-phosphate Ferredoxin Oxidoreductase, a Novel Tungsten-containing Enzyme with a Potential Glycolytic Role in the Hyperthermophilic Archaeon Pyrococcus furiosus, Journal of Biological Chemistry 270, 1995-04, עמ' 8389–8392 doi: 10.1074/jbc.270.15.8389
- ^ Enrique Martínez-Carranza, Gabriel-Yaxal Ponce-Soto, Luis Servín-González, Luis David Alcaraz, Gloria Soberón-Chávez, Evolution of bacteria seen through their essential genes: the case of Pseudomonas aeruginosa and Azotobacter vinelandii, Microbiology 165, 2019, עמ' 976–984 doi: 10.1099/mic.0.000833
- ^ Yan Zhang, Jiao Jin, Biyan Huang, Huimin Ying, Jie He, Liang Jiang, Selenium Metabolism and Selenoproteins in Prokaryotes: A Bioinformatics Perspective, Biomolecules 12, 2022-06-29, עמ' 917 doi: 10.3390/biom12070917
- ^ Gregory V Kryukov, Vadim N Gladyshev, The prokaryotic selenoproteome, EMBO reports 5, 2004-05, עמ' 538–543 doi: 10.1038/sj.embor.7400126
- ^ Isabelle J. Schalk, Olivier Cunrath, An overview of the biological metal uptake pathways in P seudomonas aeruginosa: Pseudomonas and metals, Environmental Microbiology 18, 2016-10, עמ' 3227–3246 doi: 10.1111/1462-2920.13525
- ^ Lauren D. Palmer, Eric P. Skaar, Transition Metals and Virulence in Bacteria, Annual Review of Genetics 50, 2016-11-23, עמ' 67–91 doi: 10.1146/annurev-genet-120215-035146